您现在的位置是:Fabet > Nhà cái uy tín
Thêm 5 thuốc nội nhận giấy đăng ký lưu hành_kết quả trận thụy điển
Fabet2025-03-15 02:11:12【Nhà cái uy tín】7人已围观
简介Tin thể thao 24H Thêm 5 thuốc nội nhận giấy đăng ký lưu hành_kết quả trận thụy điển
Danh sách 5 thuốc gồm: Pharcavir,êmthuốcnộinhậngiấyđăngkýlưuhàkết quả trận thụy điển Zacutas 60, Zacutas 90, Dactasvir 30mg, Dactasvir 60mg, lần lượt có số đăng ký từ VD3-29-19 đến VD3-34-19.
Cục quản lý Dược yêu cầu cơ sở sản xuất và cơ sở đăng ký thuốc có trách nhiệm sản xuất thuốc theo đúng các hồ sơ, tài liệu đã đăng ký với Bộ Y tế và phải in số đăng ký được Bộ Y tế Việt Nam cấp lên nhãn thuốc.
Đồng thời thực hiện việc cập nhật tiêu chuẩn chất lượng của thuốc theo quy định. Cập nhật nhãn thuốc, tờ hướng dẫn sử dụng thuốc theo quy định tại Thông tư số 01/2018 trong thời hạn 6 tháng kể từ ngày ký ban hành Quyết định này, theo hình thức thay đổi, bổ sung giấy đăng ký lưu hành thuốc quy định tại Thông tư số 32/2018/TT-BYT ngày 12/11/2018 của Bộ trưởng Bộ Y tế quy định việc đăng ký lưu hành thuốc, nguyên liệu làm thuốc.
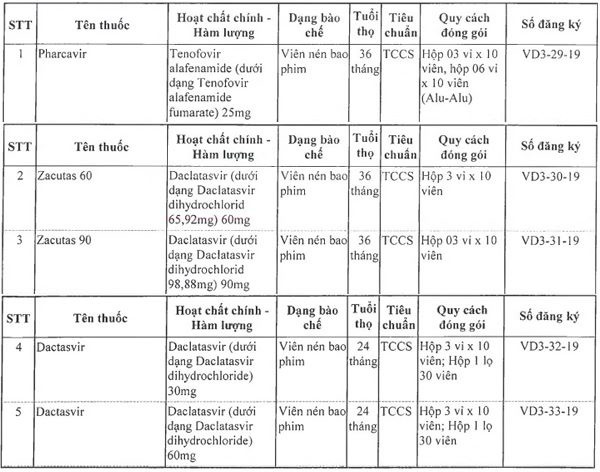 |
| Danh sách 5 thuốc mới được cấp giấy đăng lý lưu hành |
Đối với thuốc Pharcavir chứa hoạt chất tenofovir alafenamide fumarate (thuốc số 1 tại danh mục) phải cập nhật tờ hướng dẫn sử dụng theo tờ hướng dẫn sử dụng thuốc Vemlidy đã được Cơ quan Quản lý Dược Châu Âu (EMA) phê duyệt trong thời hạn 03 tháng kể từ ngày ký ban hành Quyết định này và chỉ được sản xuất, lưu hành sau khi được Cục Quản lý Dược phê duyệt nội dung này.
Các có sở sản xuất cần phối hợp với các cơ sở điều trị để thực hiện theo đúng các quy định hiện hành về thuốc kê đơn, theo dõi an toàn, hiệu quả, tác dụng không mong muốn của thuốc trên người Việt Nam.
Cơ sở đăng ký thuốc phải bảo đảm duy trì điều kiện hoạt động trong thời gian hiệu lực của giấy đăng ký lưu hành thuốc, nguyên liệu làm thuốc. Trong trường hợp không còn đáp ứng đủ điều kiện hoạt động, cơ sở đăng ký phải có trách nhiệm thực hiện thay đổi cơ sở đăng ký.
Đối với thuốc số thứ tự 02, 03, 04, 05 (chứa hoạt chất daclatasvir dihydrochlorid) tại Danh mục ban hành kèm theo Quyết định này, cơ sở phải gửi mẫu thuốc kèm theo chất chuẩn đối với 03 lô sản xuất đầu tiên để Viện Kiểm nghiệm thuốc Trung ương hoặc Viện Kiểm nghiệm thuốc TP.HCM kiểm tra theo tiêu chuẩn chất lượng đã đăng ký, chỉ được lưu hành sau khi kết quả kiểm nghiệm đạt yêu cầu.
T.Thư
很赞哦!(1)
相关文章
- Nhận định, soi kèo MU vs Arsenal, 23h30 ngày 9/3: Nuôi hy vọng
- Để một chiếc ô tô ‘lăn bánh’ cần phải trả những chi phí gì?
- ‘Mất mạng như chơi’ bởi thói quen này khi sử dụng xe tay ga
- Đại lý ôtô Honda sốt sắng mở đặt cọc lô xe vừa cập cảng
- Mỹ nói về hoạt động của Wagner, tiếng nổ lớn ở ‘thành phố hạt nhân’ Nga
- 6 thực phẩm mùa đông giúp giảm cân
- Dưỡng chất giúp đôi mắt sáng khỏe
- 'Hô biến' căn hộ 75m² cũ kĩ ở phố cổ Hà Nội trở nên đẹp lung linh chỉ với 300 triệu đồng
- Sự thật đằng sau những cảnh nóng của sao Việt
- Top ô tô sedan cũ giá chỉ từ 200 triệu đồng
热门文章
站长推荐

Siêu máy tính dự đoán MU vs Arsenal, 23h30 ngày 9/3
Giảm béo bụng: Bài tập giảm vòng hai rất dễ thực hiện

Thâu tóm Mercedes: Biểu tượng nước Đức về tay Trung Quốc

Tổ hợp khách sạn sát Hồ Gươm: Hai biệt thự cũ có bị đập bỏ?
Khởi tố vụ án buôn bán thuốc bảo vệ thực vật cấm lưu hành lớn nhất ở Đắk Nông

Trộm xe máy SH 'trong đúng 16 giây' tại Hà Nội

Tòa án tuyên chấm dứt sử dụng nhãn hiệu Asanzo, CEO Asanzo nói gì?

Chuyện phòng the: Lợi ích chuyện yêu vào buổi sáng